
El CIBERDEM estará representado por Manuel R. Benito de las Heras como conferenciante invitado a la 79th edición del Congreso de la American Diabetes Association (ADA). El investigador, que ha recibido recientemente el Premio Alberto Sols 2019 en Diabetes, en reconocimiento a su carrera científica, participa en la sesión del martes 11 de junio por la mañana dentro del Simposio dedicado a “Beta-Cell Organelles Talk Amongst Themselves", ofreciendo la conferencia “Pancreatic Beta-Cell Mitochondrial Dynamics and Mitophagy in Type 2 Diabetes and Beyond”.
La American Diabetes Association (ADA) está considerado como el Congreso más importante a nivel mundial. Tiene lugar estos días -del 7 al 11 junio- en San Francisco (EE.UU) y reúne a médicos, clínicos, investigadores, enfermeros, dietistas, farmacéuticos, psicólogos y otros profesionales altamente cualificados en el campo de la diabetes de los cinco continentes. Sus 17.000 inscripciones lo convierten en el escenario perfecto para mostrar al mundo los últimos avances científicos en diabetes.
La participación del Dr. Benito de las Heras demuestra que la American Diabetes Association ha considerado su investigación entre las más novedosas y relevantes del momento en el campo de la Diabetes.
Parte del trabajo que desarrolla Manuel R. Benito de las Heras dentro del CIBERDEM y la Universidad Complutense de Madrid está enfocado en las células beta pancreáticas como responsables de la progresión de la diabetes tipo 2 (DM2). Algunos de sus últimos resultados y conclusiones preliminares son presentados estos días en el Congreso internacional.
“Estamos tratando de entender si las células β pancreáticas podrían establecer una comunicación intercelular y cómo podría influir en la patogénesis de trastornos neurodegenerativos como la enfermedad de Alzheimer” señala el investigador.
Algunos trabajos anteriores han descrito que la demanda alta de insulina en la etapa prediabética obliga a las células β pancreáticas y causa ER y / o estrés oxidativo, lo que conduce a una disfunción en proteínas plegadas como la amilina (IAPP). “Vimos que los agregados de amilina humana (hIAPP) mal plegados se acumulan en el citoplasma de las células β pancreáticas, lo que aumenta el estrés del RE, afecta la autofagia y afecta la dinámica mitocondrial y la mitofagia” añade.
Tal y como ha estudiado el equipo de investigación de Manuel Benito, respecto a otros resultados de las células neuronales que sobreexpresan una isoforma de sinucleína alfa proagregante, esta acumulación de proteína tóxica que las células no son capaces de eliminar, podría secretarse en vesículas extracelulares llamadas exosomas.
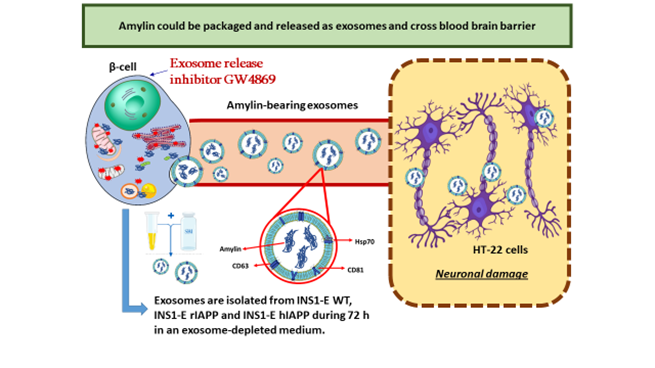
Los exosomas son micro vesículas de alrededor de 30 a 150 nm, y generalmente son secretadas por células como la comunicación intercelular, que contienen ARNm, miARN o proteínas diferentes. “Recientemente, hay algunas evidencias sobre el papel de los exosomas en las enfermedades neurodegenerativas como un posible sistema de desintoxicación para la alfa-sinucleína y el aclaramiento de beta-amiloide” explica el investigador.
“Hemos comprobado que las células hIAPP INS1-E pueden segregar exosomas que contienen una gran cantidad de amilina tóxica. Los agregados de amilina co-localizados con beta amiloide en el parénquima cerebral de los pacientes con Alzheimer y DM2 nos han llevado a la hipótesis de si este mecanismo de desintoxicación podría convertirse en un vínculo entre las células β pancreáticas y las neuronas, y qué tipo de efecto podrían tener los exosomas en las neuronas” explica el profesor.
El trabajo que ha desarrollado el Dr. Benito sugiere que los exosomas eliminan los agregados tóxicos de la hoja beta de amilina generados en las células INS1E hIAPP mediante un mecanismo de desintoxicación. “En este sentido, estamos generando un nuevo modelo de ratón que expresa hIAPP (TghIAPP) en un fenotipo de DM2 (iLIRKO), para explorar los efectos de los agregados de hIAPP y el papel de los exosomas in vivo”.
Estos exosomas podrían ser un vehículo para llevar estos productos tóxicos a otros tipos de células, agravando o acelerando los procesos neurodegenerativos, y estableciendo un posible enlace trópico nuevo e inexplorado entre la DM2 y las enfermedades neurodegenerativas.